Medische beeldvorming helpt vaak bij het succesvol diagnosticeren en behandelen van kankergezwellen. Met name magnetische resonantiebeeldvorming (MRI) wordt veel gebruikt vanwege de hoge resolutie, vooral met contrastmiddelen.
Een nieuwe studie, gepubliceerd in het tijdschrift Advanced Science, beschrijft een nieuw zelfopvouwend contrastmiddel op nanoschaal dat mogelijk kan helpen om tumoren gedetailleerder in beeld te brengen met behulp van MRI.
Wat is contrast?media?
Contrastmiddelen zijn chemische stoffen die in menselijk weefsel of organen worden geïnjecteerd (of ingenomen) om de beeldvorming te verbeteren. Deze preparaten hebben een hogere dichtheid dan het omringende weefsel, waardoor contrast ontstaat dat wordt gebruikt om beelden weer te geven met bepaalde apparaten. Voorbeelden van veelgebruikte contrastmiddelen zijn jodiumpreparaten en bariumsulfaat, die bijvoorbeeld worden gebruikt bij röntgenonderzoek. Het contrastmiddel wordt via een hogedrukspuit in een bloedvat van de patiënt geïnjecteerd.
Op nanoschaal blijven moleculen langer in het bloed aanwezig en kunnen ze solide tumoren binnendringen zonder dat ze tumorspecifieke immuunontwijkingsmechanismen activeren. Verschillende moleculaire complexen op basis van nanomoleculen zijn onderzocht als potentiële dragers van CA naar tumoren.
Deze nanocontrastmiddelen (NCA's) moeten correct verdeeld worden tussen het bloed en het te onderzoeken weefsel om achtergrondruis te minimaliseren en een maximale signaal-ruisverhouding (S/N) te bereiken. Bij hoge concentraties blijven NCA's langer in de bloedbaan aanwezig, waardoor het risico op uitgebreide fibrose toeneemt als gevolg van de vrijgave van gadoliniumionen uit het complex.
Helaas bevatten de meeste momenteel gebruikte NCA's samenstellingen van verschillende soorten moleculen. Onder een bepaalde drempelwaarde hebben deze micellen of aggregaten de neiging te dissociëren, en de gevolgen hiervan zijn onduidelijk.
Dit inspireerde onderzoek naar zelfvouwende macromoleculen op nanoschaal die geen kritische dissociatiedrempels hebben. Deze bestaan uit een vetkern en een oplosbare buitenlaag die tevens de beweging van oplosbare eenheden over het contactoppervlak beperkt. Dit kan vervolgens de moleculaire relaxatieparameters en andere functies beïnvloeden die gemanipuleerd kunnen worden om de geneesmiddelafgifte en specificiteitseigenschappen in vivo te verbeteren.
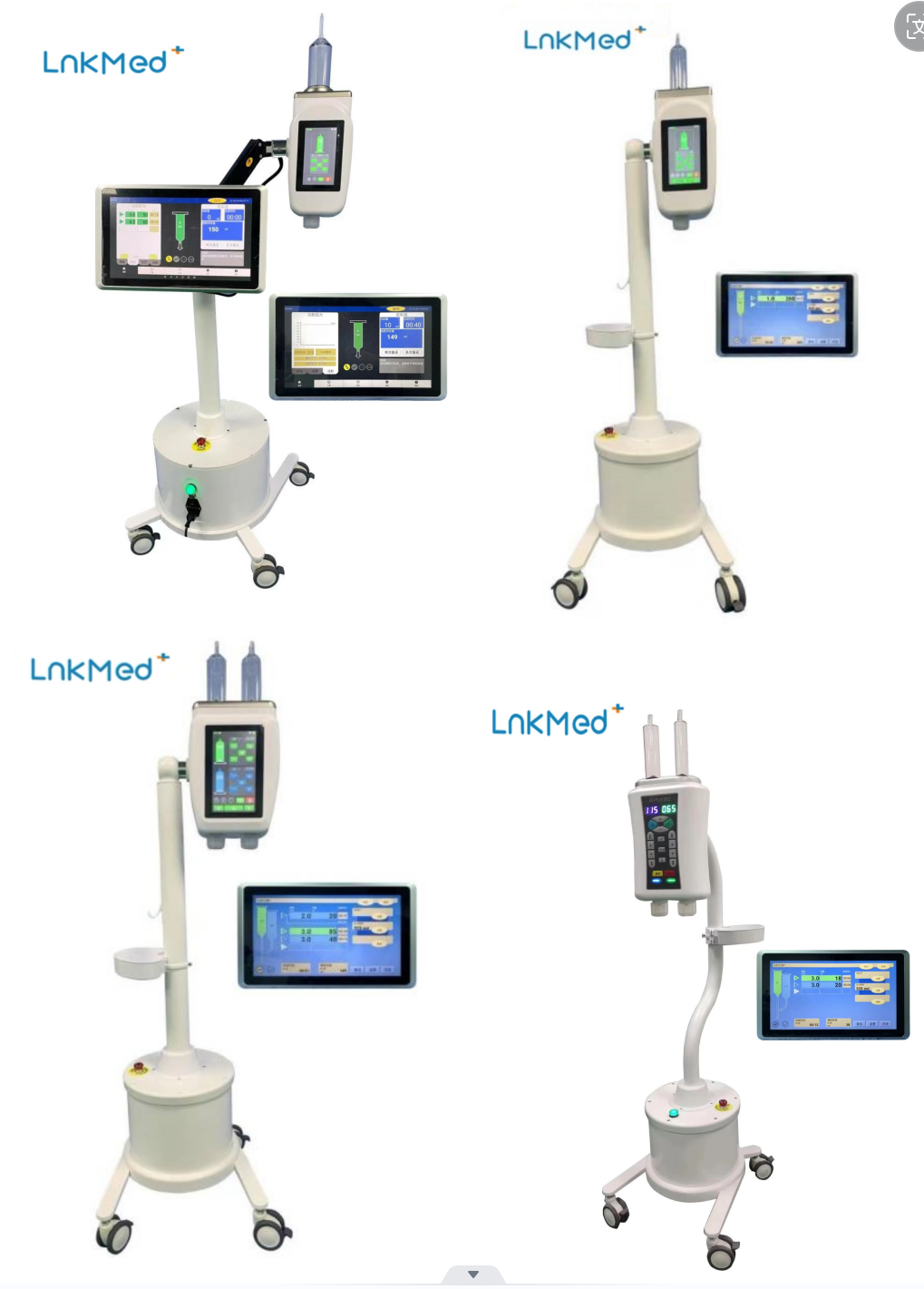
Contrastmiddelen worden doorgaans via een hogedrukinjectiesysteem in het lichaam van de patiënt geïnjecteerd.LnkMed, een professionele fabrikant die zich richt op onderzoek en ontwikkeling van injectoren voor contrastmiddelen en bijbehorende verbruiksartikelen, heeft zijnCT, MRI, EnDSAOnze injectoren worden zowel in binnen- als buitenland verkocht en zijn in veel landen door de markt erkend. Onze fabriek kan alle benodigde ondersteuning bieden.verbruiksartikelenMomenteel populair in ziekenhuizen. Onze fabriek hanteert strenge kwaliteitscontroleprocedures voor de productie van goederen, snelle levering en een uitgebreide en efficiënte after-sales service. Alle medewerkers vanLnkMedWe hopen in de toekomst een grotere rol te spelen in de angiografie-industrie, hoogwaardige producten voor onze klanten te blijven ontwikkelen en patiënten de beste zorg te bieden.
Wat laat het onderzoek zien?
In NCA is een nieuw mechanisme geïntroduceerd dat de longitudinale relaxatietoestand van protonen verbetert, waardoor scherpere beelden kunnen worden geproduceerd bij veel lagere concentraties gadoliniumcomplexen. Een lagere concentratie vermindert het risico op bijwerkingen omdat de dosis contrastmiddel minimaal is.
Door de zelfvouwende eigenschap heeft het resulterende SMDC een dichte kern en een complexe, drukke omgeving. Dit verhoogt de relaxiviteit, omdat interne en segmentale beweging rond het SMDC-Gd-grensvlak beperkt kan worden.
Deze NCA kan zich ophopen in tumoren, waardoor het mogelijk wordt om met behulp van Gd-neutronenabsorptietherapie tumoren specifieker en effectiever te behandelen. Tot nu toe is dit klinisch nog niet gelukt vanwege het gebrek aan selectiviteit bij het toedienen van 157Gd aan tumoren en het handhaven van de juiste concentraties. De noodzaak om hoge doses te injecteren gaat gepaard met bijwerkingen en slechte resultaten, omdat de grote hoeveelheid gadolinium rond de tumor deze afschermt van blootstelling aan neutronen.
De nanoschaal maakt selectieve accumulatie van therapeutische concentraties en optimale distributie van geneesmiddelen binnen tumoren mogelijk. Kleinere moleculen kunnen de haarvaten verlaten, wat resulteert in een hogere antitumoractiviteit.
“Aangezien de diameter van SMDC minder dan 10 nm is, zijn onze bevindingen waarschijnlijk te verklaren door de diepe penetratie van SMDC in tumoren. Dit helpt om het afschermende effect van thermische neutronen te omzeilen en zorgt voor een efficiënte diffusie van elektronen en gammastralen na blootstelling aan thermische neutronen.“
Wat zijn de gevolgen?
"Kan de ontwikkeling van geoptimaliseerde SMDC's ondersteunen voor een betere tumordiagnose, zelfs wanneer meerdere MRI-injecties nodig zijn."
"Onze bevindingen benadrukken het potentieel om NCA nauwkeurig af te stemmen door middel van zelfvouwend moleculair ontwerp en betekenen een belangrijke vooruitgang in het gebruik van NCA bij de diagnose en behandeling van kanker."
Geplaatst op: 8 december 2023